 ���в�ѧ
���в�ѧ
���в�ѧ��
1.��ȾԴ ��Ҫ����֢״��HBV��(AsC)�ͼ��������Ҹβ��ˡ�AsC���������ࡢ�ֲ��㣬��Я��ʱ�䳤������Ҫ����Σ�յĴ�ȾԴ���䴫Ⱦ�Ե�ǿ����Ҫ�벡������ָ��(ѪHBeAg��HBV DNA��DNA���ø)�Ƿ������йء�Լ��3%��HBVЯ���ߣ�Ѫ��HBsAg(��)��������������HBV���ƣ�Ϊ����Ĵ�ȾԴ��
2.����;�� ��Ҫ�Ǿ�ѪҺ��ĸӤ���������нӴ������������ڲ��˵�Ѫ����Һ��������֭����Һ����Һ��������������ɼ��HBsAg��������10-7ml HBsAg( )��ѪҺ����ʹ���߸�Ⱦ��
(1)��Ѫ��������עHBV( )ȫѪ��Ѫ����Ѫ��Ʒ���ʹ50%���˷�����Ѫ���ҸΡ����涣ҧ����Ŀǰ����ȷ�е����в�ѧ֤�ݡ�
(2)ĸӤ���������ҹ����е�AsC����ĸӤ�����γɵĽ�20%���ҹ�HBsAg( )�и��е�HBeAg�����ʸߴ�20%��30%��HBeAg����ĸ��������Լ��70%��90%��ΪAsC���������ڸ�ȾHBV�����³��ڻ�����������ĸӤ��ֱ�����ַ�����Χ���ڣ����ڸ�ȾԼռ5%��15%��ĸӤ���ˮƽ������ҪΪ�������нӴ����¡�
(3)�ճ��������нӴ�������������HBV������Ը�Ⱦ��Ҫ���Դ���;������;��������Ƥ�����Ĥ������Ļ����ϲ���ʵ�֡�����в���HBV��
(4)�ԽӴ��������������ѽ�HBV��Ⱦ�����Դ�������֮һ�������߸�ȾHBV�Ļ�����������������ߣ����Σ�ն�(RR)Ϊ3.7���۲�һ������Ů��HBsAgЯ����Ϊ10.4%������������Ϊ2.8%��һ�龫ҺHBV����������ż66.7%��Ⱦ��HBV����Һ������Ϊ31.6%��
(5)ҽԴ�Դ�����ͨ����Ⱦ����ͷ�����ꡢ�ھ��ȴ��������ˡ�Ҳ��ͨ��AsC��Ⱦ���������˻�ҽ����Ա��
3.��Ⱥ���� ��Ⱥ��HBV�ձ��У���Ⱦ���ͬһ���͵�HBV�ɻ��һ��������������������HBV�в��ֽ�����������
4.��������
(1)�����ֲ����Ҹγ������Էֲ������������ʲ�ͬ���¿ɷ�Ϊ�ߡ��С��Ͷ���������������ŷ�������ͰĴ�����Ϊ��������(��ȺHBsAg������Ϊ0.2%��0.5%����HBs������Ϊ4%��6%)����ŷ���ձ���ǰ�����������͵��к�����Ϊ��������(HBsAg������2%��7%����HBs������20%��55%)���й��������Ǻ��ȴ�����Ϊ��������(HBsAg������8%��20%����HBs������60%��95%)����1995�������ȫ��������������в�ѧ���������ҹ���ȺHB-sAg������Ϊ9.8%����-HBs������Ϊ27.4%���Ҹ���������Ϊ57.6%��HBsAg������ũ��(10%)���ڳ���(8%)����ȫ����Χ���������ϸ߱��͡���������״̬��
(2)�����ԣ���һ�����������ں����Եļ����ԡ�
(3)�Ա�������ֲ����Ҹεĸ�Ⱦ�ʡ������ʺ�HBsAg�����ʾ���ʾ�����Ը���Ů�ԣ�����HBs�����������Ů�Ը������ԡ��ҹ��Ҹεĸ�Ⱦ�ʡ������ʺ�HBsAg�����ʵ�����ֲ����ֳ������߷壬��һ���߷���10����ǰ���ڶ�������30����40�꣬40���Ժ�HBsAg�������������������½�����-HBs������������������������
���������Ҹ�������Ӥ���й㷺Ӧ�ã���Ч��Ԥ���˶�ͯHBsAgЯ��״̬�����Ϻ�ij��1��10���ͯHBsAg�������½�Ϊ1.4%���Ҹ�����Ľ�������ʾ���ޱȵ�������
(4)��ͥ�ۼ��ԣ�HBsAg�����Եļ�ͥ�ۼ����������HBeAg�����ߣ���ͥ�ۼ����������ߡ�
(5)����ֲ����濹�ȵȵ��飬HBsAg������ں���Ϊ15.3%���ء����������ߣ��ֱ�Ϊ26.2%��24.0%���衢ά��ͣ��ֱ�Ϊ7.0%��5.3%��
(6)AsC��ԭ���Ը�ϸ���Ըΰ�(HCC)���ҹ���������ǰհ�Ե���ָ����HBsAg(��)����HCC������Ϊ247.62/10��(��)��Ϊ21.01/10��(P��0.01)��
 ��������
��������
�������ƣ�HBV���������߹��ܵĸ�Ⱦ�������Բ��䣻���쳣���߹������������Ը������Ըβ���HBV������ϸ��������(cytopathogenic)������HBV��Ⱦ���뾭����������Ӧ�����䣬��ʹ������չ��
1.��������
(1)�������أ����ײ�����Ⱦʱ�Բ�����ԭ������Ӧ���벡�������ͷ���������ء�HBV��Ⱦʱ������Ĥ��ԭ����Һ����Ӧ���������ѪҺ�еIJ����������Ժ˿Ǻ���ø��ԭ��ϸ������Ӧ�����������Ҳ��ϸ����
�ٲ��������������֯�������˶��ڸ�ϸ������IJ�����ԭ������������ϸ������Ӧ��һ����Ϊ�Ǹ�ϸ�����˵ľ������ء�ϸ������Ӧ����ֵ�����ϸ���ڸ���֯�еĽ����Բ�ͬ�̶ȵ���֯�ƻ�����֯�ƻ�Ҳ����Һ������أ������ڷ�Ӧ���塢����Ͳ��塢�����߸�������γɺ�����֯�ڵij�����
���ײ�����Ⱦ������ԭ���ǶԲ�����ԭ������Ӧ����£������ڲ����������������ݣ�����������������HBV��Ⱦ����������Ҫ���á�
����Tϸ����CHB(����������)���˵Ĵ��������ܰ�ϸ��������ڣ�����Ѫ���ܲ��ַ�ӳ�����ڸ��ڵ����߹��̣��и��Ƶı����ƵIJ��ˣ�����CD4 /CD8 ϸ�����������ϸߣ���ʾԭλ�ĸ���-�յ���CD4 Tϸ�������ܾ�HBcAg���������CD8 CTL��ϸ�������ԡ���Բ����з����Thϸ����¡����70%��Th1ϸ������PBMC�еĽ�4%�����ڸ��ҵ�CD4 ϸ��Ⱥ�е�Th1�ܶ�Խ��������IFN����ˮƽԽ�ߣ�ϸ��������ҲԽǿ�����ڵ���֢�����еĿ�ԭ�̼�������������Щϸ����������Th1ϸ������CHB�ĸ�ϸ�����˻��ơ�
��ԭ������ʶ��һ���������߷�Ӧ����ʼ��Tϸ�����帴����п�ԭ��ʶ��Tϸ�����帴����(�ܰ�ϸ��Ĥ�ϵ�TCR��CD3�����)��������ԭ���ϸ�����ϸ������Ŀ�ԭ��MHC�����ء�HBV�˿ǿ�ԭ�ĺ˿ǵ��ױ�λֻ�Ǿ�ϸ���ڴ����ġ�8��16���������һС�ι���(��λ��)��CD4 Tϸ����ʶ��λ������HBc/eAg�ĵ�AAl-25��AA61-85��λ��CD8 CTLʶ���������δ��ֽ綨����ͬ���塢��ͬMHC��Ⱦ�ߵIJ�ͬ��Ⱥ��Tϸ�����ں˿ǿ�ԭ�����������ϵ�ʶ���λ�в��IgG-��-HBc�ɲ����ڱ�HBcAg�����HBc����CTL��HBV�п�ԭ��ʶ����ʹHBV��Ⱦ����������֮һ����HBc�����ƶԸ�ϸ����ϸ����ЧӦ����ĸ�ױ�������Ŀ�HBc��ɷ���ͬ�������á�
HLA(��ϸ����ԭ)���ƣ���APC(��ԭ���ϸ��)��ʵĿ�ԭ����/HLA-�����ֱ����CD4 Tϸ��CD4/HLA-����ӵĦ�2-�ṹ�����ϣ��Ӷ���ЧӦ���ϸ��֮������õ������ԡ���Ըβ��IJ��˵ĸ�ϸ��Ĥ�н�ǿ��HLA-I����ɸ���Ч����Tϸ���ṩ�˿ǹ��ġ�
ͬ����APC�п�ԭ����HLA-�����γɸ����壬�����ϸ�����档Thϸ����������CD4����ȥ̽��APC�����HLA-������TCRȥ̽��еĻ�����ԭ�ģ�����CD4 Thϸ����ʶ����̡�
TCR����/HLA������֮��Ľ�ϲ��ȶ�����CD4������HLA-��Ħ�2���ν�ϡ�CD8������HLA-I�Ħ�3���ν�ϣ��γ�����ṹ���ܱ��֡�TCR�븴����֮���Ҫ�ĽӴ�ʱ�䡣���⣬��Щϸ��������ϸ��𤸽���ӣ�ϸ�����ճ����ǿ��ϸ����ķ�Ӧ��
��MHC(��Ҫ��֯�����Ը�����)����������Ŵ�ѧ��������HBV��Ⱦ��չ����Ҫ���أ����Խ��Ͷ�HBV�е�������졣HBV��Ⱦ����HLA�������ٴ���������������в��ٱ��棬������һ�µ��������HBV��Ⱦ�������Ի����ص�HLA������A3-B35��A29��A2��B8��B35��DR3��DR7������ص���B5��B8��DQwl��DR2��DR5��
ϸ�����ӣ�ϸ��������ϸ���䴫��������Ϣ������γ�һ�����ߵ��ڵ�ϸ���������磬ͨ����һ�������ϸ������Ӧ�𡣼��Ը���ʱ�ڸ�Ⱦ�ֲ���IFN��������Ⱦ��ϸ���ͷ�IFN����Χ���ʣ�������ڸ�ϸ���Ŀ�����״̬�����Ը���ʱ�ɽ���ĵ�����ϸ����������ʵ��ϸ��ԭλ�ͷŵ�ϸ�����ӣ�������Ӧ��ϸ����ֳ����ά���������á�
IL-2��Th����IL-2�ͱ���IL-2R���ǵ���ϸ�����ߺ���Һ���ߵ����Ļ��ڡ������Ը������Ըβ���IL-2�������٣�������Դ��IL-2��ܾ�������ʾIL-2R�ı����ཱུ�ͣ����Ѽ��ٵ�IL-2Ҳ���ܳ�����ã�������ܳ�ּ���Tϸ����ֳ����CHB��˥������������IL-2�յ������ܰ����Ӽ����ɱ��ϸ��(LAK)����Ҳ���͡�
�����أ����Ը���ʱ��Ⱦ��ϸ���ͷ�IFN����Χ���ʣ�������ڸ�ϸ���Ŀ�����״̬������HBV��Ⱦʱ����IFN���������ͣ���˥�߲��˵���ͣ�����Ѫ���д�������IFN���������ӡ�
�����������Ӧ�����Ҫ�ɵ��˾���ϸ��������TNF-��������ǿ����𤸽���ӵı��������֢��ϸ����ЧӦ��TNF-�����ܶ���ϸ��������������ܼ���ϸ����������ϸ����
ת���������Ӧ�������ʹ�����ij���άϸ���ı��ͷ���ת�������������T��Bϸ���ɲ����ϴ�����TGF�¡�һ����ԣ�TGF�¶����Լ��ʵ�ϸ����̼����ã�������Ƥ��Դ��ϸ�����������á�
��CHB���˵�PBMC����ΧѪ����ϸ�����м���TGF-��1����HBcAg�̼�������IFN-�úͿ�HBc�������������ã�����HBcAg�̼���PBMC��ֳ��TGF-�¶Կ�ԭ���������졢ϸ������Һ���ߣ����������ò����������𣻶�Tϸ����Bϸ���͵���ϸ���������ƣ�Ҳ������HLA-I���Ƶ�CTL����HBV��Ⱦ��ϸ����ϸ�������ԡ�
TGF-��1���������֬ϸ���������ʵ��ף��յ���ԭ������ϸ������ʳɷֵĺϳɡ�����ϸ�������ף�Th1��ϸ�����Ӱ���IL-2��IFN-�ú�TNF-�£���Ҫ�漰ϸ�����ߣ�Th2��ϸ��������IL-4��IL-5����Ҫ������Һ����Ӧ��
CHB��CHC������
�����������ڽ���ϸ�����в�ͬ��ϸ���������ͣ���ʾ��ͬ�Ŀ���������Ӧ����Ϊ����CHC��Th1Ӧ��ռ���ƣ�����HCV��
���������������ƣ�����������ȫ�������HCV��Ⱦ���Ǵ��ڵ��ɵIJ���ˮƽ����CHB��ǿ��Th2�ͽ�����Th1Ӧ��ֻ�ܱ��ֵ�Ч�ʵĿ�����ЧӦ���ʸ�Ⱦ�����ڳ��ڳ�����
����������HBV��Ⱦ�ĸ���֯��ʼ�����쿹ԭ-Tϸ����Ӧ�����Է�������֢ϸ��������ϸ����������á���֢��һ����Ҫ������TNF�����CHBʱIFN-�ô̼�TNF-���������ӣ�����AsCʱ������TNF-�����������⣬CLD��IL-1����������λ����ά������������ء�������������ȫӦ��IJ��ˣ������ƿ�ʼ���8��10����֢�����ͬʱPBMC����TNF-����IL-1���ӣ���������Ӧ��IJ�����Щ���Ӳ����ӡ��ڴˣ�T�ܰ�ϸ��ͨ���ܰ�����IFN-�á�����M��ͨ����������TNF-����IL-1������ϵͳ����������
�ڿ��������ߺͲ���������Ⱦ���������߷�������Ҫ�Dz�������Ĥ��ԭ����Ĥ����Ӧ�𣺿�HBs���ڲ��������Ļָ��ڼ�������������Ը�Ⱦ�г��֣������к��Կ��壻�����ܷ�ֹ�������Ŷ���������ϸ����Ȼ������HBsͨ���γɿ�ԭ�����帴���Ҳ����һЩ��HBV��Ⱦ�йصĸ����ۺ����ķ������ơ�
���������ԣ���������������ϵͳ�ڽӴ�ij�ֿ�ԭ������ġ�ֻ�Ը��ֿ�ԭ�������������Ӧ��״̬����HBV�����������ڸ�ȾС���з������ձ顣���γ�AsC����������
�������ܿ��ܵĻ��ƣ�A.����ϸ���д�����ͬ�����Ե�ϸ����¡������������HBsAg��Ӧ��ϸ����¡�Ӵ�HBsAg�ϵľ����أ����Ƿ�������Ӧ�𣬶��DZ���������ƣ�B.��CD8 Ts������ǿȱ����HBsӦ��C.ĸ��HBeAg��������HBV��Ⱦ�������������ã�D.Ѫ���и�Ũ�ȵĿ�ԭʹ�����¡��Bϸ���Ľߣ���������������ɱ�������ԭ�ķѣ����߿�������CTL���߸��ɵIJ������Ľߡ�
������Ⱦ��A.�������죺���ڱ�����������ݣ�B.��Ⱦ���������ⲿλ������������Ⱦ��ijЩ������֯�ܰ�ϸ�����Ե����ijЩ���͵�ϸ��������HLA���ӣ�������������Щ��λ���ƣ��Ϳ����ӱ��������������Ϊ���������Ⱦ����Դ��C.�������ܣ�����HBV��Ⱦ���˴��в�ͬ�̶ȵ����������ԡ�
(2)��ϸ�����������������֯������Ҫ��CTL��������;����ϸ��������CD 95L��ϸ��������Ҳ���ɵ��˾���ϸ����TNF-��;����ϸ�����������������ж����Ļ��ƣ���ͬ�ķ���������������ϸ��������������ʽ���������DZ�����ʽ����������������̬���������治ͬ��ϸ���������ض���ϸ��������ʽ����������һЩ��ͬ������·�Σ��ֿ����ߵĽ��߲��������
��ϸ��������ӣ�CD95L��CD 95���FasL��Fas��������ϸ����ϸ��������ӣ�CD95L�����壬��CD95�������塣CTL�����CD95L��ϰ�ϸ�������CD95���������ϸ���ĵ�����
TNF-����TNR-�£�TNF-�� ��Ҫ��M�ղ������Ƕ����Ի��Ч�Ե�ϸ�����ӣ�����֢��Ⱦ���ݿ�������Ҫ���á�
��ϸ����ЧӦ��CD95L��CTL�ϵ�CD95L���ϸ���ϵ�CD95��ϣ��Ӷ������ϸ���ڲ�����ɱ����
��CD 95���źŵ��µ�����������һ;����CD95���俹����������彻����CD95����������;��������ϸ����Ca2 ��Ҳ�����д���ӵĺϳɡ�
CTL��ϸ����ЧӦ��IL-2�����ģ������IL-2�����Ƶ����ķ�����
����ϸ���İ�Ĥ���������ѳɵ���С�屻M�ջ����ڸ�ϸ�����ɣ����������������ﲻ��й����һ���������ơ�DNA������ϸ��������תȾHBV�ĸΰ�ϸ��ϵHep G2 2 15ϸ������δתȾ��Hep G2ϸ�����ܵ������ӵĴ̼���
�����Ը��ĸ�ϸ����HB���HCC�ĸΰ�ϸ��Ҳ����CD 95L��ϸ���ġ���ɱ���͡�ͬ����ɱ����һ�ַ����߹��������������ʽ�������Ƕ�HBV�������IJ������ơ�
TNF-������Ҫ��M�ղ�������鵼��ϸ��������ȡ���ڰ�ϸ���������ԡ���ת�����Ƽ����߾�ͪ����ϸ����TNF-������������е��͵ĵ���������
�����Ը���ʱ�ĸ�ϸ��Ҳ����TNF-����HBx��ת������TNF-�������ӣ�TNF-��ɱ��ȡ����HBV�����ˮƽ���ڸ߱����ϸ��ϵTNF-��������ϸ��������
�۸������ϸ��������
A.���Ժͼ��������ף���������ĸ�ϸ�������IJ��������У������ͻ�����ͬʱ������
�������������ķ�չ������һС��ģ�Ϳɹ��ο���HBsAgת����С��ע��HBsAg�����CTL���������ΰ����Է�չ��4h��CTL���ϸ����ֱ������ã���������HBsAg���Ը�ϸ���������������ֹ㷺ɢ�ڵĵ���С�壻4��12h�е�����ϸ���������ӣ�������������֢������Ӵ����ǿ�ԭ������ܰ�ϸ����������ϸ��������CTL�ľֲ���ϸ������ЧӦ��ע���24��72h��������ϸ�����������ԣ������㷺�ֲ�������СҶ��ͬʱ���������ϸ����CTL����ԭ�̼�����IFN-�ã���������������ϸ�����������ڵ�M�գ�����CTL��ϸ������ЧӦ����������ϸ�������������������������HBsAg���졢MHC-I���Ƶ�CTL��ʶ��ԭ������IFN-�ã�����M�պ����ġ�
TNF-���ɾ����������(ȡ����ʵ��ϵͳ)ɱ����ͬ������ϸ��ϵ��������2��ʱ�࣬����ϸ������Ϊ�����ij�ʼ�ں͵����㷺��ϸ������Ϊ�����ĽϺ��ڡ�
B.���Ը������Ըβ����������Ը��ײ��˸��ڽ�����ܰ�ϸ���ɼ��CD95L�����ܱ���CD95L���ܰ�ϸ����������ϸ����������Ҫ��ЧӦϸ����CD95L��CD95���DNA���˺͵������Խ�������֢�������������ϲ����ڸ��ڵĴ�Ⱦ���̣��ֲ����������CTL����CD95L����CD95�鵼��ϸ���������Dz����Ը����������������������������Ը���ʱ��ϸ��Ҳͬʱ����CD95��CD95L���ڵ������������в����ǰ�ϸ����Ҳ��ЧӦϸ����
��ϸ����CD95L��CD95����ij̶�����֢����Ļ��һ�¡���������֯���ԡ�����CH�����Ը��ף�������������ڽ�������֢������������ϸ�����С�����CH��Ϊ�С�ǿ�ȱ���ڽ�������֢���ж�������ϸ������СҶ��Ҳ��ɢ�ڡ����������Էֲ���
CH�ϲ�����LC�ͻ��LC���н�����֢��CD95L��CD95Ҳ�����С�ǿ�ȱ����HCC������������������������������Ļ��ơ�
(3)�������죺�����Ⱦ���첡�����ȾҰ�������������������Ӧ��ͬ�����첡��������ѧ������У��ӱ���Ȼ�����Ļ�������������ߡ���ҩ�������ԡ��ı䷢�����ƣ������ı���������֯�����ԡ������������������Dz����������²���ת�����Ҫ���ء�
��HBV��ǰc/c���������죺ǰC���γ�һ�����нṹ(��װ�źŦŸ�-��ṹ)���ǰ���ǰ������RNA�����裬���ܽ���������28��TAG����ļ��������ʡ�G1 896��T1 858���������Ÿ�-��ṹ�IJ��ȶ�����ԣ�ntl 896��G����ΪAʹ�ɣ���ṹ��Ϊ�ȶ�����ǰC/A83���������HBV��Ⱦ��Ȼʷ�Ľ��ձ��������HBeѪ��ת�������У���Ԥʾ���仺�⡣
��HBV��C�������ξۼ����죺C�������ķֲ�������������ּ�����AA48-60��AA84-101��AAl47-155��13��18��9���������3С�������У���������λ�нϸߵ�����ʡ�
C���������������������Ӧ�����ҪĿ�꣬�벡��ķ�����Ⱦ��ϸ���������ء�C���������������HBV�������Ը�Ⱦ�����У������ӱ���������IJ��ԣ�ʹ��Ⱦ����������ʹ������ء�
��HBV��C���������ӱ��죺C����������(cp)�ı���ҲʹHBcAgȱʧ���ѷ���ntl 762��A��T��ntl 764��G��A����HBeAg(��)�����ͺͼ����������йء�
cp����ntl 643��1849���ṹ���ܽϸ��ӣ���X�����C�����ǰC���в����ص���DRl����ǿ�Ӣ����������ڣ�ǰC mRNA��ǰ������C/P mRNA���ڴ˴���ʼ��cp�ɺ������ε�������(CURS)�ͻ�������������(Bcp)�����ֹ��ɣ�Bcp����ntl742-1849���ε�108�������ᣬ��������DRl����2��mRNA����������ܱ��أ���ʾ��Щ������ȶ��Dz������������衣
����Ⱦcp�������Կ��иߵζȵ�HBV DNA�������ȾҰ������������⣬��ʾ��Щ���첢������Ӱ��HBVǰ�������ת¼��
cp�����ʵģ���HBe״̬����������δ������ص��ض��ı䡣ntl 762��ntl 764�����ż���ڼ��������ף�Ҳ�������Ը����������Ըβ�����δ����HBeAg�����͡�
2.�����仯
(1)�����Ը��Ļ��������仯��
�ٸ�ʵ�ʵ������Ա�ͻ�����
A.��ϸ��ˮ�����ԣ�����������䣬����ʱ������ֲ��ϸ�����ı䡣
B.��ϸ�����������������Ի������ܽ��Ի�����ǰ�������Ϊ������С�塣���ܽ��Ի����������䷶Χ�Ͳ�λ�IJ�ͬ�ɷ�Ϊ��״���������Ի�������СҶ��������黵�����Ǵ�黵����������м�����������Ի�����
C.��ϸ��֬�����ԡ�
D.��ϸ���ٵ���ëϸ���ܺ�С�����ٵ���
E.������ϸ�������Ա仹����֬���س����������Կ������ԡ��˿��ݵȡ�
F.С������Ƥϸ�����ԡ����������䣬���м������ң���Ƥϸ���������ϸ�������ڸ�ϸ����Ƭ����ʱ�ɼ�С���ܴ���������������Ƥϸ�����ϸ�����С�
G.�ڸ�ϸ�����ԡ�����ͬʱ�����и�ϸ�������������������γɼ�СҶ��
�ڸμ��ʲ�������Խ���
A.����֯����ϸ��������ҪΪ�ܰ�ϸ����������ϸ���ͽ�ϸ���Ľ����ɼ��ܰ�ϸ��������ϸ���������ո�ϸ������������Ծ��
B.�����������������γɼ���ά�����ر��dz�����м״����ʱ����ά��֯����м״����֮��֢��Ӧ�����СҶ�����Ի������γ��µ���ά��������ϸ����Ƭ����ʱ�����ݵ���״֧�����ת��Ϊ��ԭ��ά��������ά���γɡ����Ը���ʱ��������֬ϸ����������ת��Ϊ��άϸ�����б���ָ������ʱ������ϸ����ɲ�����ԭ��ά��
(2)���Ͳ����Ը��IJ����仯
�ټ������Ͳ����Ը��ף�����Ϊ
�δ���Ѫ������֯����Ȼ��ж���֢����ʵ�ʵIJ�����Ҫ�Ǹ�ϸ��ˮ�����ԣ����ϸ���������Ի�����㡢��״���������и�ϸ����ëϸ�����ٵ��ȡ�
�����Բ����Ը��ף�
A.������Ը��ס�����ԭCPH��CLH������CAH��G1��2��S0��2����ʵ�ʵ��̶Ƚ��ᣬ����ϸ��ˮ�����ԣ��㡢��״����������������ϸ�������ֲ�����СҶ�ܱ���֢���ɰ���������м״��������СҶ�ṹ����������
B.�ж����Ը��ס��൱��ԭ����CAH��G3��S2��3���λ������֢����СҶ��Ե��֢���ԡ���СҶ��Ե�������Ե���м״������Ϊ�ж����Ը�����Ҫ��������СҶ����ƻ��ɴﵽ50%����ά��֯����ϸ���������뵽��СҶ�ڡ�������СҶ�ṹ�Ա���ԭ�еĻ���������
C.�ض����Ը��ס��൱��ԭ����CAH��G4��S3��4�����Ϊ���ء��������֢����ά��֯�������أ��������ض���м״������
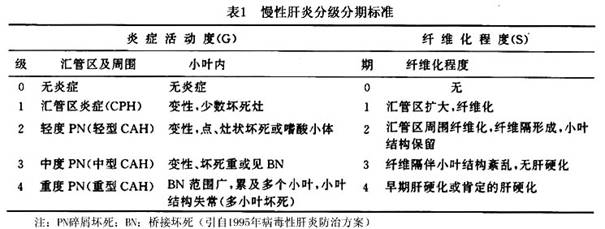
����������̬ѧ�ص㣬�����Ը���ʱ����֯����֢��Ƚ��зּ�������ά���̶Ƚ��з������1��
�������ף�
A.���������ס���������Ϊ��ϸ�������Ի��Ǵ����Ի�������������ɴ��ʵ��֮2/3���ϡ��ڴ����Ի�������Χ��ϸ�������ضȵĸ�ϸ��ˮ�����ԡ�
B.�Ǽ��������ס��ڸ�ϸ���¾ɲ�ͬ�Ĵ�Ƭ�����Ļ����ϣ��������Եĸ�ϸ��������
C.���������ס������Ի��Ǽ��������IJ����ı��⣬���ɼ���ԭ�е����Ը������µij¾ɵ���ά����ͬʱ���Կ���СҶ��Ե���ϸ����ڱ�Ե�����Ե���м�������Žӻ�����
 �ٴ�����
�ٴ�����
�ٴ����֣�DZ����6�ܡ�6�£�һ��Ϊ3�������ҡ�
1.����������
(1)����
�������ף������̿ɷ�Ϊ3�ڣ��ܲ���2��4���¡�
����ǰ�ڣ��ϻ�����ҪΪ��ʳ�����ĵ�θ����֢״�������������к�����֢״��ż�ɸ��ȡ�����
��ʹ��������Ѫ�岡�����֡����ڳ���������2�ܣ�
�����ڣ���Ĥ��Ƥ����Ⱦ���ԣ���������2���ڴ�߷塣
�������ֺ��Ƚ��ˣ�ʳ����ת�����ֲ���������֢״�ڶ������Դ��ڡ�
�δ�����������ߵʹ��ѹʹ��Լ��5%��10%�IJ���
Ƣ������ΧѪ��ϸ��һ���������Եͣ�ALT(Ѫ������ᰱ��ת��ø)�������ߣ����ڳ���2��6�ܡ��ָ��ڣ�
�������ˣ�����֢״����ʧ����Ƣ�������������ι��ָܻ����������ڳ���4�����ҡ�
(2)������
�������ף����컺��֢״��������
����ǰ�ڱ��֣����ٲ���֢״�����ԣ����ղ���Ѫʱ��ż������Ѫ��ALT���ߣ����˶���3�������ָ���Լ��5%��10%תΪ���Ը��ס�
2.���������� ���ײ��̳������꣬������䷢�����������ʱ���֡�֢״���ֶ���������������Ǩ�Ӳ�����������������֢״���������Ϊʳ��ȱ�������͡����ġ�
����������ȡ����������з������������ʡ��������ۡ������ı䡢����仯ʱ֢״���ء����ֲ����е��ȼ��������ұ��֣���ͷ�衢
ʧ�������λ���˯��ע���������С����������ˡ�������ŭ���������ʡ����������ȡ����ֲ��˿��г�Ѫ������Ϊ������Ѫ���dz�Ѫ��Ƥ�³�Ѫ����ٰߡ������������κ��Ծ�֢״���С��ض����Ը��ײ��˽���״���½����ɳʸ��Բ��ݣ�����Ϊ��ɫ�ް�����������ɼ����ơ�
֩��������
Ƣ�״����ʵ��еȻ��Ӳ���д���ߵʹ��Ƣ��ɽ������״��ֲ��˷����ڷ������ң����ֶ�ë�����غ��ή���������鷿��������ͷɫ�س��ţ��鷿�ɴ������������Ӳ�顣ʵ���Ҽ����ʾALT�������ط�����������ߣ�AST�����Ŷ�����ת��ø���������ߣ����ֲ���r-�Ȱ���ת��ø���������������ѽ�ø(ASAL)����������øҲ���ߡ�������ø�����̴����Լ���ʱ����ʾ�������ء��������������鼰�ͺ�2hѪ�嵨֭��ⶨ�ɽ������ط�ӳ���ಡ�䡣���ض����Ը��ײ����嵰��(A)���ͣ���(G)���ߣ�A/G��ֵ���ã�����IgG�����ߡ���Ѫøԭ�İ����ڽ϶̣��ܼ�ʱ��Ӧ�������س̶ȣ���Ѫ����V���������١����ֲ��˿ɳ����������壬�翹�˿��塢��ƽ�������壬�������忹�壬���ʪ���Ӽ��Ǵ�ϸ�������ԡ�
����ϵͳ���ֿɷ����ڲ����Ը����κβ��ڣ������Ը���Ϊ���������ϵͳ���е����ס������ס�θ�ס������ȣ�����ϵͳ������Ĥ�ס����ף����������С�����ס���С�����ж��ȣ�ѭ��ϵͳ���н���Զද���ס�
�ļ������İ��ȣ�ѪҺϵͳ����
ѪС��������������ϸ��ȱ��֢��
�����ϰ���ƶѪ��
��Ѫ��ƶѪ�ȣ�Ƥ���ɼ����Ӥ��������Ƥ��(Gianotti��)�����������沿���κ�ߵȣ���ϵͳ����
��Ĥ���������ס�������ס�����-�����ۺ����ȣ������йؽ��ס��ؽ�ʹ��֢�������Ը���ʱ����ϵͳ���ֵķ��������������йأ��ٲ������ַ�������Բ�����Ⱦ�ķ�Ӧ�������߸�������γɺͳ������ۻ���ϸ�����߷�Ӧ����IJ��䡣�̷ܼ��ڸ�ʵ����Ӱ�졣
3.����������
(1)���������ף��ֳƱ������ס��������Ƽ���
�������ף������鷢չѸ�͡���10���ڳ��־���֢״�����˷ܡ��Ը���Ϊ������������ʡ���ҹ���������IJ��ȡ����ﲻ�塢
������֢״��
����Ѹ�ټ����������Ѹ����С�����˻���������������䡣�����г������Գ�Ѫ����
��Ѫ�������ȡ�
��ˮ��������ˮ���ʸߣ����ֲ��˷����Բ������ڷ��������
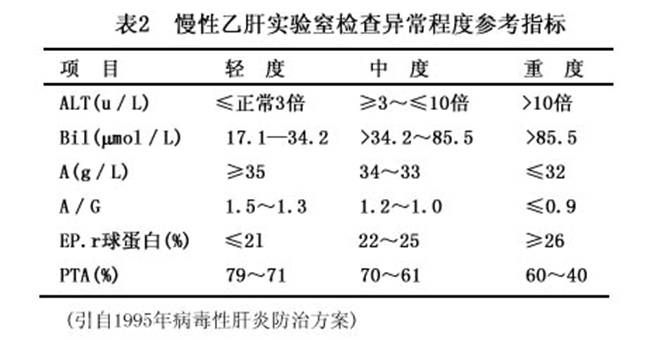
��Ѫѹ����������˥�ߡ�������ΧѪ��ϸ���������ߣ�Ѫ�嵨���أ�171��mol/L����ƽ��ÿ����17.1��34.2��mol/L���ٶ�Ѹ���������������˳���ø�����������Σ�ء�Ԥ��������̳�������3�ܡ�
(2)�Ǽ��������ף��ֳ��Ǽ��������ס�����ʱ�����Ƽ���
�������ס�֢״�����أ����˼��ȷ���������ʳ��ȱ����Ƶ������Ż�£�
�������̣�����
��ˮ���ν��������С��
����Ѹ��������Ѫ�嵨���ش���171��mol/L�����Գ�Ѫ������Ѫøԭʱ���ӳ������С��40%��Ѫ�嵰���ͣ�A/G��ֵ���ã�����ALT������������ø����룬AST/ALT��ֵ��1�������Բ��������ڲ��̺��ڣ����ڻ��ɳ������س�Ѫ����������ң���-
�������������ظ�Ⱦ������
������˥�������̽ϳ����ɴ����¡����ֲ��˿ɻָ������չΪ������
��Ӳ����
(3)���������ף��ٴ����ֿ����Ǽ��������ס������������Ը��ס�
��Ӳ�����Ҹβ���Я��״̬�Ļ����ϣ����������ظι������������Ը����������������Լ��ض���Ϊ���������ף��������ͬ���Ի��Ǽ��������ף�����ʬ��֤ʵ��ϡ���Ҫ����Ϊ
���������Լ����Ѫøԭ��Ƚ������½��������������˵Ĵ���
��ˮ���������ظ�Ⱦ�����Ծ����ĵ�������ҡ����Ͳ��˳��е���Ѫ֢������ͨ�������ϰ��������������Ƶļ�ǿ���������ϲ��˲����ָ����Բ������������ǰ���֣�����
����������Ѫ����-
�������������ظ�Ⱦ��������
4.�ٵ����� �����ٵ����������Ƽ���
�������ף����Ծ�֢״���ᣬ
���������Լ��ز�����3�����ϣ�����Ƥ�����������ɫ��dz�������ڿɳʻҰ�ɫ��
�δ���Ѫ�嵨�����������ߣ���ֱ�ӵ�����Ϊ����R-�Ȱ���ת��ø����������ø�����̴���Ѫ�嵨֭������ߡ���������ALT�������ߣ����ܿ��½�������ø����롣���ֲ�����Ժʱ��Ѫøԭ����½�����������ά����K
1��3��7���Ѹ�ٵõ�������B������������֡�
 ����
����
���ƣ�
1.���Ը������� ���Բ����Ը���һ����������̣�ע���ʵ���Ϣ��֢״���أ��л�����Ӧ�Դ���Ϣ�������嵭������Ӫ�������������յ���ʳ��ע�⵰���ʼ�ά���ص����롣����Ż����Ӱ���ʳ������������Ӧÿ����Һ���䡣���ݲ��˲�ͬ���������Ӧ����ҩ�ɷ����֤ʩ�Σ����ڻ���֢״�����̲��̡����ٲ���֢�������ġ�����������Ը��ײ���Ҫ���������ơ������ڲ���Ǩ�ӳ���8�ܣ�Ƶ�������߿ɿ��Dz��ÿ������Ʒ���һ������Ӧ��������Ƥ�ʼ��أ�������Ӧ�öԸ���������ʳ��ҩ�
2.���Ը�������
(1)������ҩ�
�ٸ�����(IFN)��IFN��Ŀǰ��õĿ�����ҩ������Ʋ������ƾ��й����ԡ�����ԡ����������Լ����������ԡ���-IFN�ij��ü���Ϊ3��5MU/�Σ�ÿ��3�Σ��Ƴ�4��6���¡�Ҳ�ɲ���3��5MU/d��1��/d��1���º��Ϊÿ��3�Σ��Ƴ�ͬ�ϡ�������Ӧ��1��2���Ƴ̡���С����(��1Mu/��)�ﲻ������Ч�����������(�磾10MU/��)���׳��ֲ�����Ӧ�������Ʋ������ܵIJ������ӡ��ʵ��ӳ��Ƴ̿��Լ��ٷ��������ƺ�Լ��40%�IJ��˿ɻ�ó־����Ʒ�Ӧ����HBV D
NA(�ߵ��ӽ���)��ʧ��HBeAgת����ALT��������������������ֲ��˿�-HBeת�������1�꣬�Ա����ȶ����䡣����-IFN���ƺ�
HBsAgת������Լռ10%���ң�һ�㷢���������л����ƽ�����3�����ڡ��־�����ЧӦ���������ƽ�����һ�꣬�λ����ʾ������ǰ�����Ժ�ת����־�����ЧӦ�IJ��ˣ�Լ��20%��30 %�ɸ����������߶���Ϊ���Ʋ�����֣����ظ����ƣ�һ���������÷�Ӧ��
�ڵ����ᰢ������(Ara AMP)����ѡ��������D
NA���ø���Ӷ����Ʋ���D
NA�ϳɡ��÷���ÿ��10mg/kg������ע�������ע��6�����������Ƴ�1���¡�ͣҩ��������
�۰�����Τ(ACV)�����ں���������Բ���D
NA���ø�����������á�����Ϊÿ��15mg/kg��������ע��30��Ϊ1�Ƴ̣�����������ظ��Ƴ̡�
���������������������(Lamivudine��3TC)Ϊ����ऺ�����������Ʋ�����ת¼ø������ʵ����ʾ��Ѽ����������ײ������������á���������Ϊÿ��100mg���ڷ�����1��2�������ƺ��������HBV D
NA��ת����ALTҲ��֮�½���ֹͣ���ƺ�������������Τ(Famciclovir)Ϊ�����ʺ����������ŷ�ޡ��Ĵ����Ƕ������о�����Ϊ��HBV����Ч����3TC���ơ�
������Τ��(Ribavirin)��Ϊ�����ἡ��(IMP)����ø���Ƽ�������IMP���Ӷ���ֹ��������ϳɡ������IFN�������Ʊ�������ǿ��Ч��Ҳ�ɵ�������IFN�п�ҩ�Բ��������˼���10��15mg/(kg d)����ע������ע��0.8��1.2g/d���ִοڷ����Ƴ�3��6���¡���������ҩ���������Ѫ��ƶѪ���ʵ������ɻָ���������Ѫ������ˮƽ���ߣ�����ͣҩ��
��좼�����(PFA)��Ϊ�����������������
RNA��D
NA�ϳ�ʱ�������ڷ�ת¼ø������D
NA���ø���ԡ�����Ӧ��60mg/(kg d)��������ע������2��3�ܡ��������ϵͳ������Ӧ�������ܲ����������ҩ��
�߿�ζҶ���飺����꪿�������ҩ��ζ�ࡢ�����������Ȼ�̼�Ͱ����������յ��ĸ�ϸ�����Ծ��б������ã��俹HBVЧ�ܣ�ʵ��������ϴ���ҩ��600���֣����ز�ͬ���ɼ�ʱ�䲻ͬ����Ч��Ҳ��ͬ���б��������Ҷ����ӻ���ɳ�ǿ���ǿ���������á�
Ŀǰ���õĿ�����ҩ��ֻ������HBV���ƣ��Ӷ�������֢��ԣ������ϲ��������ã��Ը�ϸ������HBV�ij��������۱պϻ���D
NA(cccD
NA)�������ã���ͣҩ��CCCD
NA�����³�Ϊ��������ת¼��ģ�塣
(2)���ߵ���ҩ��
��������(Thymosin)���÷�5��20mg/d����ע�Σ��Ƴ�2��3���£������˹��ϳ�28��������Ħ�-������(�մ���)���÷�Ϊÿ��1.6mg��ÿ��2�Σ�Ƥ��ע�䣬�Ƴ�6���£���ʹ��������HBeAg��HBV D
NAת�����۸��������д���������������ظεı���(160mg��ÿ�ջ����һ�Σ�����)��
����������(Levamisole)���÷�������150mg/d���Ƴ�4��8�ܡ���������Ϳ����Ӧ�÷��㡢������С���÷���5ml��ÿ��2��Ϳ����Ƥ�����Ƴ�3��6���¡�
�����������ߺ��Ǻ���(I
RNA)�÷���1��4mg��ÿ��2�Σ��Ƴ�3��6���¡�
�ܰ�ϸ������-2(IL-2)���÷�������IL-2 10��U/d������ע�䣬28��Ϊһ�Ƴ̡������Ӧ�ÿɳ��ֶ��ġ�Ż�¡�һ���Է��ȡ�ˮ�ף����صĵ�Ѫѹ����ʱ��������ȫ��ͣҩ�����ʧ��
��������Ƥ�ʼ��������������������ҸΣ��������˫ä�����յĶ������ٴ��۲죬������Ч�����ҿ����к���
����ҩ��ȡ�����ߵ���ҩ����߶���ע��Һ������Ϊÿ��40mg������ע�䣬����20�죬��Ϣ10�죬���ظ�3���Ƴ̡�ͬʱ����Ҹλ�������5��g��ÿ2��1��Ƥ��ע�䣬6��Ϊ1�Ƴ̡��㹽���ǿ������IFN��������ǿ��Ч��ÿ��8mg������ע�䣬8��Ϊ1�Ƴ̡���������轶��ǡ���ݾ�˿��
����ע��Һ�Ⱦ��е������߹���֮��Ч�������ݲ����ʵ�ѡ�á�
(3)���ν�øҩ��:
��ǿ������
ǿ�������÷���40��120ml����
������Һ�о��㣬1��/d��ALT������������ͣҩ���Է�ֹ���������ڴ���Ӧ��ʱ�����˳�����̴��������á�
������Ϊ
�ʲ�����������ø��������ǿ������ÿ��30ml(150mg)ϡ�ͺ��ע���ڷ�Ϊÿ��450mg���ִη��á�ע������ͬǿ������
�ڸ����飺��ALTЧ��������ÿ��4ml��ע��������ͣҩ����ֹ������������Ӧ��
����ζ�Ӽ�
����˫�����裺ǰ�߸��ݲ����������ã�����ÿ��20��45mg���ִη��á�ͣҩ��ALT�������軺������ͣҩ��
�ܴ���ݣ���������Ʒ30g�����߰24mg��3��/d������2�ܼ��ɼ�ALT�½����ι��������˼�������ͣҩ��
���Ŷ������þ���÷���10��20ml����
������Һ�л������㣬1��/d�����ڽ���Ѫ�嵨���أ����Ƹι�����Ч�������ڸ����Բ����˵����ѡ�
��
�����������÷���200mg��3��/d��12��Ϊ1�Ƴ̡��������ж��ġ�Ƥ������ȸ����á�
(4)������ά��ҩ��μ�����Ӳ�����֡�
(5)���������Ƶ��о���
�ٵ��������ƣ�Ӧ���ִ�ҽѧ���\��������Ч������ҩ�������Զ������ӡ����ص��ȣ���һ���İ������彻��������ؽ�����ҩ�����͵������ٻ��ϸ�����Դﵽ����Ŀ�ĵ�һ�����Ʒ������˷�����ѡ���Խ�ǿ�������ԽϺá�ҩ������С�����Ե͡��������Ч���ŵ㡣Ŀǰ���������о�����֬��������أ�֬���嶬���IJ����������ҸΣ�����Һ���ǵ������嵼��Ara-amp���о�Ҳ���б��������ָ�ҩ����Ϊ����������ǿ���������ýϴ�Ŀ�����ҩ���ʵ��Ӧ���ṩ�˿ɿ�;����
���Ҹ�������������о�����
��ͨ���ı俹ԭ�ݳ�;�����������ܶ��������Ӧ�𣬴Ӷ�������������״̬��������߸���������������;�����ѳ�����ʾ������Ч����
��D
NA�������ڲ����Ը��ķ��Σ�������Ŀ�Ļ��������ֱ�ӽ��ֵ������ڣ�ʹ�������ڽϳ��ڵر���Ŀ�Ļ��Ӷ�������Һ��ϸ�����߷�Ӧ���������Ƚ��ȶ���������ԭ�ԡ���������������Ӧ�ã������俹ԭ��ʷ�ʽ��һ�����粻ͬ���п��ܴ����������ܣ��ʼȿ�����Ԥ�������п����������ơ�����Tiollaais(1997)��С��ע�ܹ�����HBV��Ĥ��������D
NA�����������������߶���������˿��壬��-HBs�ζȴ���100IU/L��ͬʱ�ɼ�ϸ�����߷�Ӧ��ǿ���������Ʒ����д����о��Ρ�
�ܻ��������о���
3.������������
(1)��Ѫ��Ѫ���ó������Ƽ������ضȻ��㣺��ž�ijҽԺ��8ζҩ��Ϊ��ҩ(
������
������������ݡ����顢���֡����ء���Ƥ)��ȷ����Ѫ��Ѫ���ó�������Ѫ��Ѫ�����ضȻ��㲡�ˣ�17��Э����λ350���ضȻ��㲡����Ч��Ϊ79.3%��
(2)
��ȥ������(
UDCA)�����Ს�˷�������к��������֢״���ɱ���ϸ��Ĥ�ȶ��ԣ������ϸ����֢�����Ƹι�������ëϸ����̼���η��ڣ��ٽ���֭���ڣ����ӵ�֭�������ٽ��������ˡ�ÿ��500mg���ִοڷ��������Զ�����Ӧ������������
UDCA����ΪIFN�������Ա��εĸ�������ҩ�
(3)���ͱ��ף�Ϊø�յ��������յ�����Y���ף���ǿ����ԣ��ٽ��������ɷǽ���������Ե�ת������߸�ϸ��������������ø������ëϸ����Ĥ��Na
-K
-
ATPø�Ļ������ٽ���֭����ڣ����ӵ�֭�������Ӷ������˻ơ�ÿ��90��180mg���ִη��á���ҩ�Ը�����һ�����ι��ı�������Ӧ���ã��з��������롢Ƥ��ȸ���Ӧ��Ӧע��۲졣
(4)������Ƥ�ʼ��أ����з��������������ã������ӵ�֭�������ٽ���֭��й���Ӷ������˻����á��÷�Ϊ��������ÿ��40mg����5��7�������ͣҩ���Ƴ�1�������ҡ�Ӧ����ע�ⲻ����Ӧ�ķ���������ʹ�á�
����������þ�ɴٽ���֭��й������ϩ�����˻�ֹ�����ã�������ʹ�á�
4.���Ͳ����Ը������� ��������������Ӧ��ǿ����֧�����ƣ�ʵʩ�������ۺ��Ʒ����ٽ���ϸ�����������Ƹ���ѭ������ϳ�Դ���ڶ���Ѫ֢����TNFΪ���ĵ�ϸ���������硣��ǿ����������θ��ֲ���֢�����ڱ�������Ԥ�����Իָ��IJ������ɲ����˹���֧��ϵͳ��������ʱ���и���ֲ��
(1)����֧�����ƣ�ʵʩ���ػ������ϸ��������룬��ֹҽԺ��Ⱦ��ÿ����������������2000kcal���ϡ������������⣬��
����֬����������������Դ��Һ����ÿ����1500��2000mlΪ�ˡ�
������ע
������ȫѪ������
Ѫ��(���ϸ�ɸѡ)��������Ѫ���ӡ�
ע����ڵ���ʺ����ƽ�⣬������ϡ���Ե���Ѫ֢��Ӧ����Һ���������д���ʧ�ƻ�Ѫ��ˮƽ����115mmol/L�ߣ��������3%
�Ȼ���Һ����Ѫ��֢�������л�Լ��ж����շ�����ظ����Բ�����������������£�����ÿ�첹��3��6g
�Ȼ���Һ����ʱÿ����10%
���������10ml���Σ�ÿ����200ml������ѪҺ�����貹��1g��Ӧ����Ѫ�����������ڴ�л�Լ��ж����˿ɸ���25%
������40��80ml������ע�����ڸ����ۺ������ߣ����ϲ���л�����ж�����ѪpH��7.25ʱ��������Ӧ�ü���ҩ������ɹ�����������ؼ�Ѫ֢����������Ѫ֢���ˣ���Ҫ���������Ѫ֢���ݿ˻���˥�ߡ�
(2)�ٽ���ϸ�����������ƣ�
��
�ٸ�ϸ����������Ӧ��(PHGF)���÷�Ϊÿ��80��120mg����
������Һ200ml�ھ��Σ��Ƴ�1��2���¡�PHGF��������ϸ��D
NA�ϳɣ��ٽ���ϸ������������ǿ���ո�ϸ�����ܣ�����TNF-�����ԣ������ڶ���Ѫ֢�ķ�����������ϸ��Ĥ�������ԣ������ڸι��ܵĻָ���
���ȸ�Ѫ����-�ȵ���(G��I)�Ʒ���Ӧ���ȸ�Ѫ����1mg���ȵ���10U����5%��10%
������400ml�о��Σ�1��2��/d��2��4��Ϊһ�Ƴ̡��ٴ�ʵ����ʾG��I�Ʒ��Լ������Ͳ����Ը��״�����нϺ����ã��Ǽ�����Σ����������Ͳ����Ը��ײ�����Ч����ע���쳣�����ġ�Ż�¡��ļ¡���Ѫ�ǵȲ�����Ӧ��
��ǰ������E
1(PGE
1)��Ӧ�ã�Ӧ��PGE
l 100��200��g����
������250ml�ھ��Σ�1��/d��10��Ϊһ�Ƴ̡�PGE
1�ܸ��Ƹ���ѭ�������ӸΡ���Ѫ����������TNF-�����ɣ�������ϸ����ЧӦ��ע�ⷢ�ա�ͷʹ�Ȳ�����Ӧ��
(3)���ߵ����Ʒ��������ؿ���ǿ���忹���������������Ͳ����Ը������ظ�Ⱦ�ķ�����ÿ��20��40mg��ע�Σ���160��200mg�����ջ�ÿ��2��3�ξ��Ρ�������Ƥ�ʼ��ؿɶ̳��������Ͳ����Ը������ڡ�����Ѹ�ͽ�չ���ۺ�֧���Ʒ����������ߡ������������Ͳ����Ը����ô˷������٣�Ӧ�����ɡ�
(4)��ҽ��ҩ���ơ�
(5)�����ײ���֢�ķ��Σ�
�ٸ����Բ��ķ��Σ�������ʳ�������룬���ִ��ͨ�������θ���ڻ�Ѫ�����緢�ֲ����Ƹ�Ⱦ����Ϸ������Ƴ�����Ⱥҩ��(��
С����ŵ��ɳ�ǵ�)�������ڶ��ؼ��������ɡ����ա���Ϸ�����̬�Ƽ����Է�ֹ��Ⱥʧ����
�����(Lactulose)�÷�Ϊ50%
�����10��30ml��2��3��/d������ڼ�����ÿ������2��3��Ϊ�ˡ��ͺ�����Է�ֹ���ģ�Ҳ�����ڹ೦��
�����ײ��˳���
Ѫ��֧��/���㰱����ı�ֵ���ͣ��������ϰ�����ע��Һ��ÿ��250ml��1��2��/d��������ע�����ಡ�˳������ͼ��Ի�����Լ��ж����Ӷ����ظ�ϸ�������Ͷ�������Ӧ����Ѫ�������͵���ʼ������ʱ���������ڵ����Դ�л�Լ��ж�������25%
������ÿ��40��80ml������
������Һ�о��Σ������ڸ�����ʶ�ϰ���
����ˮ�ķ��Σ������շ���ˮ�����أ���ȱ������̼��Ѫ֢����Ѫѹ����Ѫ�ǡ��͵��ס��ͼء���֢���ڶ���Ѫ֢�ȡ����ֲ��˰�����Ϣ��ͷ��̧��30o��45o���������Ѫ��������
Ѫ����ѹ�����뾲��ѹ�������ܵ����䱣����������Χ�����м��Ѫѹ��������ѹ��20kPaʱ�輰ʱ���轵����ѹ�Ĵ�ʩ����¶����������ˮ����Ҫҩ��������кã�
Ѫ����ѹ��310mOsm/Lʱ���ɿ��پ��ƣ�����Ϊ0.5��1g/kg��ÿ4��6Сʱ1�Σ����ظ���ע��Ϊ���١�����������¶����ע��϶�ɾ�ע50%
������60ml���������(����)�����������ǿ��ˮЧ����
Ѫ����ѹ����ʱ������Ч����Ӧ������
Ѫ�����嵰�ס���ˮ�Ʒ��ڼ�Ӧע��ѪŨ������Ѫѹ����������ҵȸ���Ӧ��Ӧ�������������Ƥ�ʼ��ؿɽ���ëϸѪ��ͨ�ԣ��ȶ�ϸ��Ĥ����ø��Ĥ�����ƾֲ���Ѫ������ʹCSF�������٣��Ӷ�������ˮ�ף��÷�Ϊ����������10mg��
������20��40ml��ע���Ժ����������Ҫʱ��ÿ4��6Сʱ5mg������ˮҩ����2��3�졣�����궯��鴤�߸��趫ݹ�м�0.3��0.6mg/�Σ�������ע���������(����)10mg��ע��ע��
����������Ѫ�ķ��Σ�
�鰷H
2���������������涡0.15g��ÿ��1�λ�
��������20mg��1��/d�������涡0.2g��2��/d�ڷ�����Ӧ�ô����Ƽ���������������Ѫ�ķ����������½�����Ѫ�̶����м��ᡣ��������н�������ѹ�������ã������Լ�������25%Ϊ�ȡ�ά����K��ÿ��10��20mg��������
�������ڲ����µ�
��ѪøԭѪ֢�ij�Ѫ����Ч��
��Ѫøԭ�����������������X���ӣ�����Ѫ�ɲ���V���Ӻ�ѪС�壬��Ѫ����������X���ӡ�����������Ѫ������Ѫ(DIC)ʱӦ�������շ����أ����Ⱦ���ݿ˵ȣ���ע����ѪҺ����Ч��Ҳ�ɽ������õͼ���
������
��Ѫ�����ȣ��������˽������������ݿ��߸�����Ӧ��706�ȼ����������ƣ���ʱ��ע����Ѫ����Ѫ���������Ӧ�ü�����Ӳ����ز��֡�
�ܸ����ۺ���(HRS)�ķ��Σ���������ǰ����˥�߲�������ʱ�������������ƣ����ݺ���������30ml/h���ϣ�����Һǰ�������ɼ�����Һ����Һ�����CVP��½��У��м�Һ�����࣬���·�ˮ�ס�HRSʱӦ��Ѫ�ܻ���ҩ����Ͱ���20��60mg��
���������Σ�ÿ��1�Σ�ɽݹ�м�(654-2)��20��60mg/�Σ����λ�PGE
1Ҳ��������С���˹��ʡ�����Ӧ����������ϸ����Һ������������ʹ���������ҩ�����ǿ��������������������Ѫ�����̷ּ���Ⱦ���ɼ���HRS�ķ�����
�ݼ̷���Ⱦ�ķ��Σ������ײ���ϸ���������Ⱦ����ΪҽԺ��Ⱦ��Ӧ�Ӻ���ϼ�ǿҽԺ��Ⱦ�ļ����Ρ�����ʹ�ÿ���ҩ�����ʹ�õ������ɵ�������Ƥ�ʼ��أ����ִ��ͨ����Ӧ�������ڱ��ֳ�����Ⱥƽ�����̬�Ƽ�������ҩ��ʹ��ԭ��A.Ӧ�ÿ���ҩ��ǰһ��Ҫ������ȡ�걾���в�ԭ��������B.����ԭ���Ը�Ĥ�ף���δ�õ���ԭѧ����ǰ��Ӧ����Ը������Ծ���ҩ�C.���ظ�Ⱦʱ��������Ӧ�ÿ���ҩ��ɼ��������������ҩ�D.��ҩ��Ҫ���ݸ�������״���ʵ����١�E.�Ƴ�Ҫ�㣬һ�㲻����2�ܡ�F.ע�Ᵽ���������ܡ�G.���ܹ۲����������Ⱦ��ͷ����ʱ���á�H.��Ҫʱ��ǻ�ڿ���ҩ��ע�����ơ�
���˹���֧��ϵͳ������ֲ��



 ���в�ѧ
���в�ѧ
 ����
����
 ��������
��������
 �ٴ�����
�ٴ�����
 ����֢
����֢
 ʵ���Ҽ��
ʵ���Ҽ��
 �����������
�����������
 ���
���
 �������
�������
 ����
����
 Ԥ��
Ԥ��
 Ԥ��
Ԥ��